生物医药—洁净厂房 包装区
【法规要求】
新版 GMP 正文:
第五十七条 用于药品包装的厂房或区域应合理设计和布局,以避免混淆或交叉污染。如同一区域内有数条包装线,应有隔离措施。

A. 医药制剂包装区 GMP 风险分析
少数固体制剂生产企业只完成压片、胶囊的生产,包装工序转运到国内、外其他工厂来完成。大多数生产企业同时具备制造和包装的生产能力。
以下 GMP 厂房设施风险在包装车间同样值得关注:
避免混淆:大量原辅料、包材及成品会同时存放在现场,周转频繁。
合适的环境:包装机头部位存在暴露工序,外包材发尘量大。
采取措施,避免交叉污染:同一条生产线可能生产不同产品,线-线之间不同产品潜在的相互污染,包装后工序的外包材对前工序暴露的药品和内包材的污染。
合适的物理操作空间:大量原辅料、包材及成品会同时存放在现场,周转频繁。
合适的人流、物流路线:同一条包装线,一般需要 3 个以上操作人员。半成品运输过程产生污染。
易于清洁:包装设备自动化程度高,结构复杂。
针对以上风险,我们可以通过以下厂房设施设计理念的实施,减少或消除 GMP 风险。
对内外包材,成品储存区域分别布置
隔离不同产品生产线
尽可能采用密闭生产工艺,减少走廊占用和运输中物料交叉污染
建立有序的人流和物流,保持最小量交叉
对不同的工艺单元,设置明确的暂存区
使用易于清洁的工艺设备
提供合适的生产环境
B. 工艺路线和人流物流设计
对于口服固体制剂,片剂或胶囊等半成品从中转库房通过“密闭桶”运转到包装线,翻转提升装置将“密闭桶”通过“快速接头”联接到包装线。
对于非固体产品,除了“密闭桶+真空吸料”方式,也可采用密闭管道传料系统,包材、人流、物流设计快捷,最小化交叉污染。
C. 平面布局设计
包装车间的设置,邻近生产车间和中心储存库
包装线房间要设置与生产规模相适应的物料暂存空间。
线-线要隔离设置。
前、后包装工序要隔离
设置与产品生产相适应的洁净等级房间存储模具。
办公室和维修间不能有发尘作业,尽可能远离生产区。
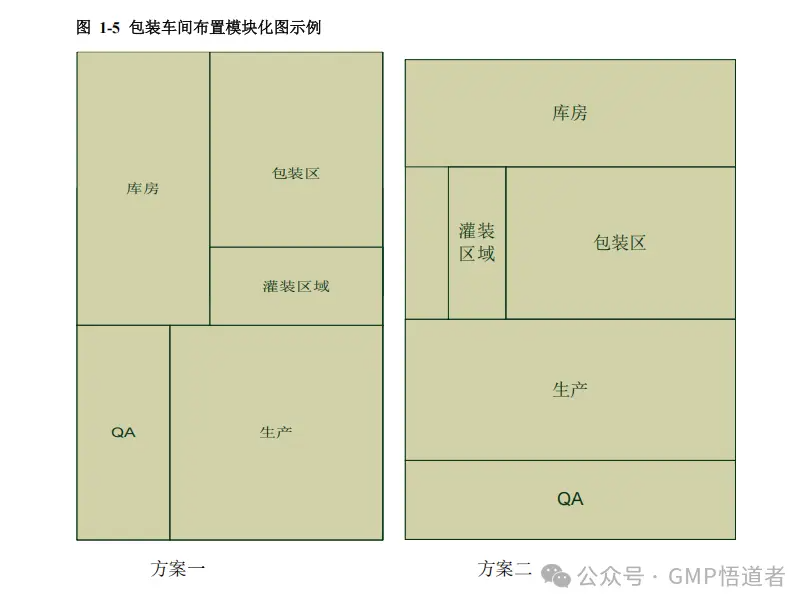
以下为包装车间布置模块化图: